1) Химические свойства
Надуксусная кислота является производным перекиси водорода и образуется пу- тем замены атома водорода на ацетильную группу. В связи с этим надуксусная кис- лота проявляет свойства как кислоты, так и перекиси1. Надуксусная кислота образу- ется при смешении уксусной кислоты и перекиси водорода и находится в растворе в равновесии с этими компонентами. При разбавлении, нагревании и т.д. легко разлагается на перекись водорода и уксусную кислоту. Перекись водорода, в свою очередь, легко распадается на кислород и воду при нагревании, взаимодействии с органическими веществами и т.д. Такие продукты разложения, как известно, прак- тически не токсичны 2,3.
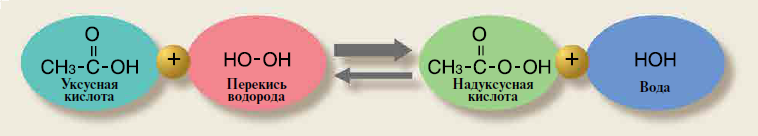
2) Антимикробное действие
Хотя надуксусная кислота и является производным перекиси водорода, она име- ет более высокую антимикробную эффективность по сравнению с последней4,5, и обладает чрезвычайно широким спектром антимикробного действия против грам- отрицательных и грам-положительных бактерий, дрожжевых и плесневых грибов, вирусов и спорообразующих бактерий при довольно низких концентрациях6-12. На- дуксусная кислота проявляет споролицидную активность даже при очень низкой кон- центрации, и ее активность сохраняется в присутствии органических соединений.
«Отличная дезинфицирующая способность надуксусной кислоты и ее активность при холодной стерилизации» была описана Фреером и Нови в 1902 году12. Надуксус- ная кислота является одним из самых мощных противомикробных препаратов и, бла- годаря своей бактерицидной активности, относится к высшей категории среди мно- гих описанных дезинфектантов, и показывает отличную эффективность почти во всех сравнительных исследованиях, осуществляемых разными учеными6. Надуксусная кислота также эффективна в отношении биопленок по сравнению с обычно исполь- зуемыми на практике дезинфектантами13.
Линам с сотрудниками сравнили бактерицидное действие препарата на основе 0,35%-й надуксусной кислоты с действием препарата на основе 2%-ного глутарового альдегида против различных кислотоустойчивых бактерий, используя суспензионный метод14. Как показано в таблице 1, глутаровый альдегид не был эффективен против M. сhelonae, выделенной из машины для мойки/дезинфекции эндоскопов, и медлен- но действовал против M. kansasii. С другой стороны, препарат на основе надуксусной кислоты действовал намного быстрее и уменьшил число тестируемых кислотоустой- чивых бактерий, в том числе для выделенных штаммов M. chelonae, на 5 порядков и более в течение 4 минут.
Сравнение бактерицидного действия надуксусной кислоты (0,35%) и глутарового альдегида (2%) на кислотоустойчивые бактерии14
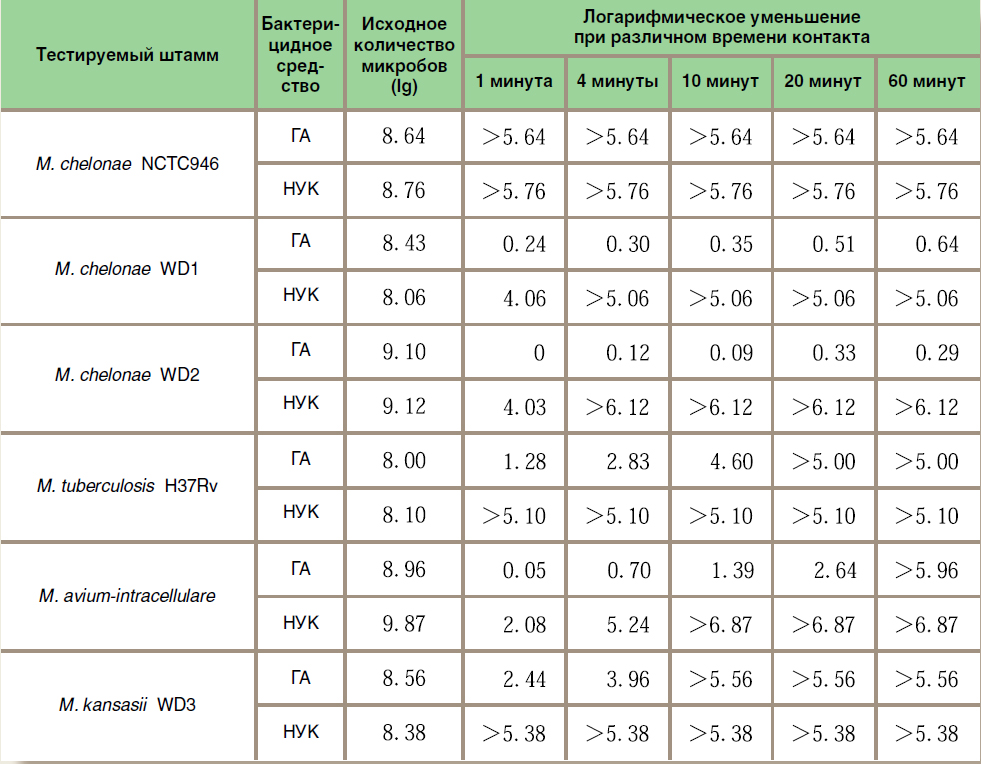
НУК: надуксусная кислота, ГА: глутаровый альдегид
WD: штаммы микроорганизма 1, 2 и 3, выделенные из машины для мойки/дезинфекции эндоскопов.
1 Ogata, Y., Chemistry of Organic Peroxides, p.100, Nankodo, Tokyo, 1970. (In Japanese)
2 Dychdala, G. R., Proc. 4th Conf. Chem. Disinfection, New York State University, Binghamton, NY, 1988, pp.315-342.
3 Block, S. S., Disinfection, Sterilization, and Preservation. 4th Ed, Edited by S. S. Block, Lea & Febiger, Philadelphia, 1991, pp.172-179.
4 Baldry, M. G. C., The bactericidal, fungicidal, and sporicidal properties of hydrogen peroxide and peracetic acid. J. Appl. Bacteriol. 1983;4:417-423.
5 Eggensberger, H., Zentralbl. Bakteriol. Mikrobiol. Hyg. [B], 1979;168:517-524.
6 Baldry, M. G. C. and Fraser, J. A. L., Industrial Biocides. Edited by K. R. Payne, John Wiley & Sons, NY, 1988, pp.91-116.
7 Sprossig, M. Resistance of Microorganisms to Disinfectants: Second International Symposium. Edited by W. B. Kedzia, Warsaw, Polish Academy of Sciences, 1975, pp.89-91.
8 Schroeder, W., Brauwelt Int. 1984;1:115-120.
9 Block, S. S., Proc. 3rd Conf. Prog. Chem. Disinfection, New York State University, Binghamton, NY, 1986, pp.1-28.
10 Roshner, D., Technical Bulletin, Hankel Corporation, 1987, p.27.
11 Dychdala, G. R., Disinfection, Sterilization and Preservation, 3rd ed., edited by S. S. Block, Lea and Febiger, Philadelphia, 1988, pp.157-182.
12 Cords, B. R. and Dychdala, G. R., Antimicrobials in Foods. 2nd Ed.,(Ed. by Davidson, P. M. and Branen, A. L.), Marcel Dekker, 1993, pp.469-537.
13 Holah, J. T. et al., Lett. Appl. Microbiol. 1990;11:255-259.
14 Lynam, P. A. et al., J. Hosp. Infect. 1995;30:237-239.
3) Механизм действия
Точный механизм действия надуксусной кислоты до конца не известен. До недавне- го времени считалось, что надуксусная кислота ведет себя подобно другим окислителям и механизм ее действия, возможно, аналогичен механизму действия перекиси водо- рода. Однако Гриспен с сотрудниками предположили, что механизм антимикробного действия надуксусной кислоты отличается от механизма действия перекиси водорода, поскольку НУК не взаимодействует с каталазой, которая разлагает перекись водоро- да15. Маркизом с сотрудниками показано, что бактерицидное действие надуксусной кислоты объясняется образованием органических радикалов и, таким образом, не свя- зано с перекисью водорода, при этом восстановленные формы меди, железа и кобальта снижают бактерицидную активность НУК в то время как для окисленных форм этих металлов, Mn2+, K+ и комплексообразователей подобного эффекта не наблюдается16. Дэвис и сотрудники предположили, что надуксусная кислота уничтожает бактерии, разрушая сероводородные (-SH) и дисульфидные (S-S) мостики в белках и ферментах при окислении17. Болдри и Фрэйзер утверждают, что протозоицидная и спорицидная активность надуксусной кислоты связана с разложением белка, при этом в белках, ферментах и других продуктах обмена веществ происходит окисление реакционно- способных меркаптогрупп и дисульфидных мостиков, а также имеют место реакции с двойными связями18. Павлова и Куликовский показали, что бактерицидная и спори- цидная активности являются следствием нарушения транспорта веществ в бактери- альную клетку19.
Установлено, что надуксусная кислота реагирует с белками и, таким образом, на- рушает химическую осмотическую функцию и транспорт веществ в белково-липид- ной мембране из-за деструкции стенок бактериальной клетки18,20. Таким образом, существует 3 различных механизма деструкции микробных клеток надуксусной кис- лотой; (1) деградация клеточных белков и замедление транспорта веществ в клетке, (2) инактивация ферментов, необходимых для обмена веществ, (3) нарушение кле- точной мембраны и ее проницаемости.
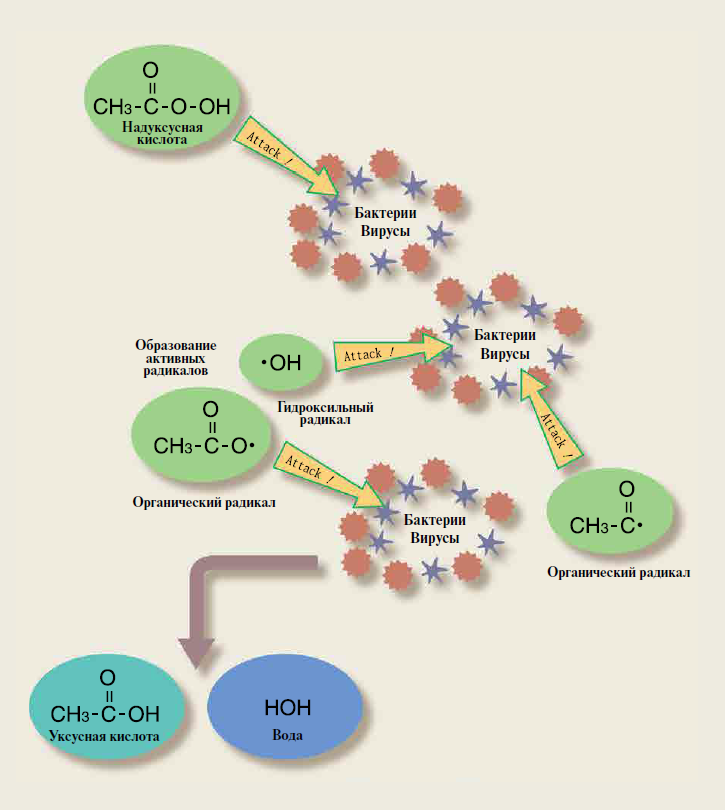
Клапп с сотрудниками (1994) в недавнем исследовании методом электронного парамагнитного резонанса (ЭПР) показали, что 5,5-диметил-1-пирролин-N-оксид (ДМПО), используемый в качестве спиновой ловушки, и антиоксиданты (витамин С и Trolox C) замедляют бактерицидную активность, и, таким образом, подтвердили, что гидроксильный радикал является бактерицидной химической частицей, образующей- ся в результате взаимодействия надуксусной кислоты с бактериями21. Учеными также доказано, что гидроксильный бактерицидный радикал при этом продуцируется в теле микроорганизма. Бактерии, культивируемые в среде, обогащенной железом, демон- стрировали повышенную чувствительность к бактерицидному действию надуксусной кислоты. Однако добавление ионов железа к смеси надуксусной кислоты и бактерий не привело к увеличению бактерицидной активности дезинфектанта. Результаты, по- лученные при дополнительном введении в смесь комплексообразователя железа и гемопротеина, свидетельствуют о влиянии их присутствия на бактерицидную актив- ность надуксусной кислоты.
Механизм инактивации вирусов под действием надуксусной кислоты исследован в работе Мейларда и др.22 с использование бактериофагов в качестве модельных струк- тур. Установлено, что надуксусная кислота вызывает изменения в белках, нуклеино- вых кислотах и строении (в капсиде и хвостовом отростке) фага F116. Малчески систематизировал вышеупомянутые механизмы действия надуксусной кислоты в своем общем обзоре23.
15 Greenspan, F. P. et al., Proc. 42nd Ann. Mig. Chem. Dec. 5-7, CMA, Washington, DC.Mfctrs. Assoc., 1955, pp.59-64.
16 Marquis, R. E. et al., J. Ind. Microbiol. 1995;15(6):486-492.
17 Davis, B. D. et al., Microbiology Including Human and Molecular Genetics, 3rd Edition.Harper and Row Publishers, Inc., London, 1980, pp.344-351.
18 Baldry, M. G. C. and Fraser, J. A. L., Industrial Biocides. Edited by K. R. Payne, John Wiley & Sons, NY, 1988, pp.91-116.
19 Pavlova, I. B. and Kulikovski, A. V., Zh. Mikrobiol. 1978;1:37-41.
20 Fraser, J. A. L., Specialty Chemicals 1987;7(3):178-186.
21 Clapp, P. A. et al., Free Rad. Res. 1994;21(3):147-167.
22 Maillard, J. Y. et al., Sci. Prog. 1997;80:287-315.
23 Malchesky, P. S., Disinfection, Sterilization, and Preservation. 5th ed. (ed. By Block,S. S.), Philadelphia: Lippincott Williams & Wilkins, 2000, pp.979-996.

